一、化学中sigma键是什么?
原子间通过电子云头碰头重叠而形成的共价键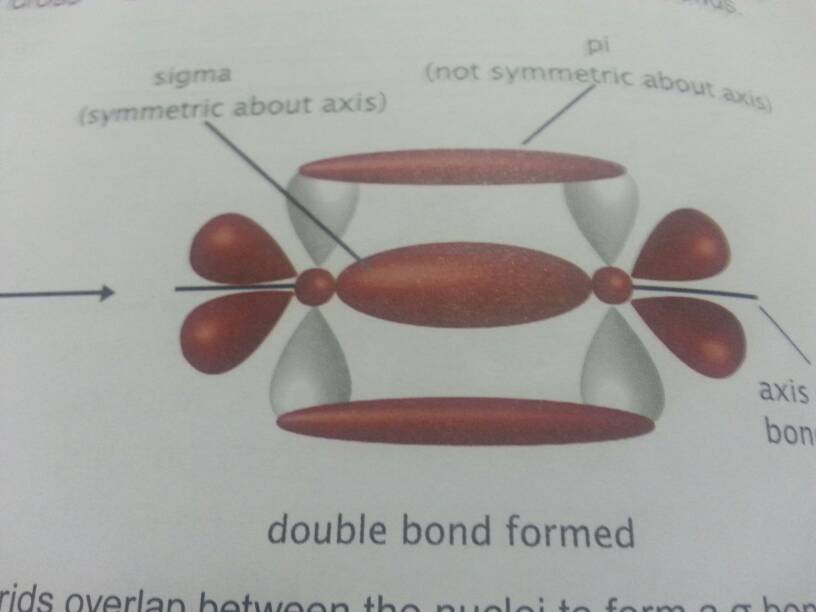
所有的单价都是σ 键,,如H2 Cl2 中的H-H,CL-CL键;双键中有1个σ 键,叁键中有2个σ 键
二、氢键属于sigma键吗
氢键不属于sigma键。
sigma键和Π键是共价键,是化学键的一种,而氢键是一种分子间作用力,不属于化学键。
氢键是一种静电作用,是除范德华力外的另一种分子间作用力。氢键的大小介于化学键与范德华力间,不属于化学键,但有键长、键能,氢键具有饱和性、方向性。化学键是纯净物分子内或晶体内相邻两个或多个原子(或离子)间强烈的相互作用力的统称。使离子相结合或原子相结合的作用力统称为化学键。离子键、共价键、金属键各自有不同的成因,离子键是通过原子间电子转移,形成正负离子,由静电作用形成的。共价键的成因较为复杂,路易斯理论认为,共价键是通过原子间共用一对或多对电子形成的,其他的解释还有价键理论,价层电子互斥理论,分子轨道理论和杂化轨道理论等。金属键是一种改性的共价键,它是由多个原子共用一些自由流动的电子形成的。
三、化学中sigma键是什么?
原子间通过电子云头碰头重叠而形成的共价键.
所有的单价都是σ 键,如H2 Cl2 中的H-H,CL-CL键;双键中有1个σ 键,叁键中有2个σ 键
四、有机化学中的σ键、α键、β键、i键和γ碳分别是什么?
σ键是沿键轴(两原子核的连线)方向以“头碰头”的方式发生原子轨道(电子云)重叠,轨道重叠部分呈现圆柱形对称沿着键轴而分布,具有轴对称特征的共价键。
比如C=C, 凡与这两个碳原子连接的键称为α键,沿着这条链往远数,依次是β键,γ键。没有i键这种说法。
形成σ键时,原子轨道的重叠部分对于键轴呈圆柱形对称,沿键轴方向旋转任意角度,轨道的形状和符号均不改变。由于形成σ 键时成键原子轨道沿键轴方向重叠,达到了最大程度的重叠,所 以σ键的键能大,稳定性高。
扩展资料:
σ键是共价键的一种。它具有如下特点:
1、σ键有方向性,两个成键原子必须沿着对称轴方向接近,才能达到最大重叠。
2、成键电子云沿键轴对称分布,两端的原子可以沿轴自由旋转而不改变电子云密度的分布。
3、σ键是头碰头的重叠,与其它键相比,重叠程度大,键能大,因此,化学性质稳定。
共价单键是σ键,共价双键有一个σ键,π键,共价三键由一个σ键,两个π键组成。
σ读音Sigma
参考资料来源:百度百科—σ键
五、化学sigma键是单键还是双键 怎么区分sigma键和∏键啊 看不懂啊
碳碳单键都是由σ(sigma)键构成的
而碳碳双键则是由一个σ和一个π键构成的,所谓σ键是由两个相同或不相同的原子轨道沿轨道对称轴方向相互重叠而形成的共价键(称为头碰头),叫做σ键。若原子轨道的重叠部分,对键轴所在的某一特定平面具有反对称性,所成的键就称为π键(肩并肩)。
六、σ键是什么?怎么读
σ:读作:sigma (西格码)
σ键是“杂化轨道理论”和“分子轨道理论”中的一种化学键名字,就像“共价键”,“离子键”一样,只不过含义更为复杂,更为精确,涉及到一些微观电子云方面的知识。如果你只是在读高中,那么是不用了解这种化学键的吧。
σ键属于“共价键”,成键两原子的价电子云沿键轴方向重叠而成键。也就是所谓的“头碰头”的成键方式。
就像在灯光下,左右手各握一个拳头“相对”,它们的影子就像是价电子云的形态,这两个影子相互重叠形成的一个“大的电子云”,即形成共价键(共享电子)。
一般的“单键”都属于这种σ键,比如C-H, O-H, N-H, C-C, C-Cl等等。
还有一种键叫π键。也是共价键,成键两原子的价电子云平行或者侧面重叠而成键,也就是所谓的“肩并肩”的成键方式。相当于两个“拳头”相平行,然后再重叠形成“大的电子云”。双键,三键中都有这种键(当然也有σ键),比如C=C, O=C, C=N等等。